Mindent az ozmiumról

Ozmium - ritka fém, a platina csoportba tartozik. Angliában fedezték fel a platina reakciójával kapcsolatos kísérletek eredményeként. Az ozmium nevet görögül adják, és fordításban "szagot" jelent. Milyen ez a nemesfém? Milyen tulajdonságai vannak és mire használható?

Történelem
Ezt az elemet Smithson Tennant és William H. Wollastan angol kémikusok véletlenül fedezték fel 1803-ban. A platina savak (kénsav és salétromsav) keverékével való reakciójával kapcsolatos kísérletek eredményeként a keletkező csapadék kellemetlen aromát fejlesztett ki, amely a klór és a rothadt retek bűzére emlékeztetett. Hasonló kísérleteket végzett Colle-Descoti, Antoine de Fourcoy és Vauquelin Franciaországban. Kutatásaik eredményeként a platinából származó oldhatatlan üledékben ismeretlen anyagot is találtak.



Az akkor még ismeretlen anyagot csibének nevezték el, de a britek kísérletei bebizonyították, hogy két hasonló anyagról van szó - az irídiumról és az ozmiumról.
Ezeknek a kémiai elemeknek a felfedezését Tennant 1804. június 21-én kelt írásos közleménye mutatta be a londoni Royal Societynek. Mengyelejev kémiai elemeinek periódusos rendszerében a fém a 76-os sorszám alatt található. A fém tiszta formájában nem rögök formájában fordul elő, ezért kémiai képlete oldott formában jelenik meg.


Az elemet másodlagos nyersanyagokból vonják ki az irídium-, platina-, platina-palládiumércektől vagy réz- és nikkelércektől való elválasztása eredményeként. Az egész elem éves termelése a világon nem haladja meg az 1 tonnát.


Születési hely
A világ legnagyobb lelőhelyei olyan zónákat érdemelnek, mint pl Urál hegyek és Szibéria Oroszországban, az északi államban Alaszka és nyugati állam Kalifornia Amerikában, Kanada Észak-Amerikában, Colombia Dél-Amerikában és néhányban Dél-afrikai országok, Ausztrália, Sziget Tasmania... Jelenleg jelentős ozmium lerakódásról van szó Bushwell komplexum Dél-Afrikában, az anyag nagy részét ott bányászják. Figyelembe véve, hogy a fém legnagyobb lelőhelyei Dél-Afrikában találhatók, ennek a ritkaföldfémnek a világpiaci árai meglehetősen magasak. Kazahsztán az ozmium-187 egyetlen jelentős exportőre a világon. Bár Kínában vannak platinaérc tartalékok, nem rendelkezik jelentős mennyiségű ozmiummal.


Az anyagot por formában tárolják, és mivel nem olvad meg kristályok formájában, ezért fizikai tulajdonságai miatt nem lehet rá bélyegezni. Ebből a fémből készült bugák gyártásához porból elektronsugaras vagy ívmelegítést alkalmaznak, valamint tégelyben történő melegítést is alkalmaznak.


Tulajdonságok
Az ozmium ezüstös kékes fémnek tűnik. Az egyik legsűrűbb elem, sűrűsége köbméterenként 22 600 kilogramm, ugyanakkor az anyag meglehetősen törékeny, könnyen törik, morzsolódik. Nagy a fajsúlya, és még meglehetősen magas hőmérsékleti behatásoknál is fényes. Paraméterei és jelentős olvadási hőmérséklete miatt nehezen megmunkálható. A természetben hét izotóp formájában létezik, amelyek közül hat stabilnak tekinthető, ezek az ozmium-184, ozmium-187, ozmium-188, ozmium-189, ozmium-190 és ozmium-192. A laboratóriumban 162-197 tömegszámú radioaktív fémizotópokat kaptak, és mesterségesen is előállítottak néhány nukleáris izomert.
Az ozmium jellemzőinél fogva minden élő szervezetre hátrányosan hat.

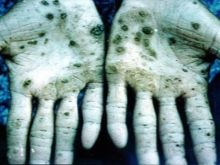
Szinte minden vegyület ezzel a fémmel károsítja a belső szerveket, látási és hallási zavarokat. Ozmium gőzzel történő mérgezés esetén visszafordíthatatlan zavarok léphetnek fel a szervezetben és halál is előfordulhat. A tudósok kísérleteket végeztek állatokon, amelyek eredménye a vérszegénység gyors fejlődése, a normális tüdőfunkció hiánya volt. Arra a következtetésre jutottak, hogy ez egy gyorsan fejlődő ödéma. Az ozmium-tetroxid, amelyet a gyógyászatban használnak, nagyon maró hatású anyag. A világ legrosszabb szaga van. Mérgezés esetén a bőr szenved, zöldre vagy feketére változtatja a színét, gyakran fekélyek és repedések kísérik, amelyek gyógyulása nagyon hosszú ideig tart.


A termelési létesítmények alkalmazottai vannak a legnagyobb kockázatnak kitéve, az összes biztonsági előírás szerint csak légzőkészülékben és speciális ruházatban dolgoznak. Minden ozmium-oxidot tartalmazó tartályt le kell zárni és a szabályoknak megfelelően tárolni. A nevyanskite ásványi anyagainak előállításához a platinát aqua regia segítségével oldattá alakítják. Ezután a keletkező csapadékot 8-szoros mennyiségben cink hatásának teszik ki - az ilyen ötvözet viszonylag könnyen porszerű állapotba kerül, amelyet aztán bárium-peroxiddal olvasztnak össze. A következő lépés a kapott massza feldolgozása aqua regiával, desztilláció az ozmium-tetroxid elválasztó berendezésen keresztül.

Az anyagra lúgos oldattal hatva sót kapunk. A sóoldat érintett hiposzulfit, melynek következtében ammónium-klorid segítségével a fém már Fremy-só formájában kicsapódik. A csapadékot mossuk, szűrjük és kalcináljuk. Mindezen tevékenységek eredménye szivacsos ozmium. Ezt követően savakkal megtisztítják, elektromos kemencében hidrogénáram alatt redukálják, majd lehűtik. Így ozmium minták elérése 99,9%-ig.


Kémiai
Ennek az elemnek a tulajdonságai a kémia szempontjából lenyűgözőek. Ezek közül a legalapvetőbbek a következők.
- Az ozmium egyáltalán nem lép reakcióba lúgokkal és savakkal. Lúgos olvadékokkal reagálva vízben oldható ozmátokat képez. A salétromsav és sósav keverékével való kölcsönhatás rendkívül lassú reakciót eredményez.
- Nagyon mérgező, még mikroszkopikus adagokban is. Különösen mérgező az ozmium-oxid, amely a platinából szabadul fel.
- Lehetetlen meghatározni a fém forráspontját, mivel különösen tűzálló.
- A porban lévő fém könnyen hevítési reakcióba lép az ilyen anyagokkal: tiszta oxigénnel, halogénekkel, kén- vagy salétromsavval.
- Különféle vegyületekben -2 és +8 közötti oxidszámok érhetők el. A leggyakoribbak a +2, +3, +4 és +8.
- Képes klasztervegyületeket képezni.
- A fő ásványi anyagok a szilárd oldatokhoz kapcsolódnak, és az irídium és az ozmium ötvözetei képviselik őket - ezek a szisertskite és a nevyanskite. Ezenkívül a syserskite más névvel rendelkezik - iridious ozmium, és nevyanskite - ozmous iridium.

Fizikai
Sűrűség Az ozmium körülbelül 22,61 gramm/köbcentiméter. A kristályok gyönyörű ezüstös fényűek, különböző árnyalatokkal a szürkétől a kékig. A tuskókban sötétkék szín jelenik meg, a porban lila. Minden fém ezüstös fényű. Az elem toxicitása megakadályozza annak használatát az ékszeriparban. A fő fizikai tulajdonságok a következők.
- Ennek az elemnek az olvadáspontja meglehetősen magas, az olvadás 3000 Celsius fok feletti hőmérsékleten lehetséges.
- A fémnek nincs mágneses tulajdonsága.
- Elképesztő szilárdság. Az ezt a fémet tartalmazó ötvözetek megnövekedett kopásállóságot, tartósságot, korrózióállóságot és mechanikai igénybevétellel szembeni ellenállást érnek el.
- A forráspont 5012 ºC.
- Mohs keménysége 7.
- Vickers keménysége 3-4 GPa.

Alkalmazások
Maga az elem jelentős költsége miatt ezt a fémet ritkán használják tömegipari termelésben. Az ozmiumot elsősorban a vegyiparban használják, ahol katalizátorként használják. Az ozmium-tetroxidot egyes gyógyszerekben használják. Laboratóriumi vizsgálatokban élő szövetek festésére használják, biztosítja a sejtszerkezet megőrzését.
A repülőgépiparban ozmiumot használnak a légiközlekedési és rakétatechnikai berendezések elektronikus berendezéseiben, valamint a gyártásban nukleáris fegyverek. A mágneses tulajdonságok hiánya miatt a fémet a márkás órák, például a Rolex gyártásához használják. Az ozmium és platina ötvözetét akkor használják, ha sebészeti implantátumok létrehozása Pacemakerek vagy pulmonalis billentyűk.
Ezenkívül az ozmiumot a mikroszkópiában és nagy pontosságú műszerek előállítására használják.



Érdekes tények
- Az ozmiumban körülbelül 770 GPa nyomás alatt az elektronok kölcsönhatásba lépnek a belső pályákon, az anyag szerkezete változatlan marad.
- Ozmium a kőzetekben az érctelepek teljes tömegének fél százalékát tartalmazza.
- A nagy sűrűség miatt a fém megjelenése és tényleges súlya nagyon változó. Tehát egy ezzel a fémporral megtöltött 0,5 literes műanyag palack nehezebb lesz, mint egy 10 literes vízzel megtöltött vödör.
- Ez a fém az öt legtöbb között van drága.
- Egy három uncia ozmium ára üzleti titok, nyílt forrásokban hozzávetőleges árat talál 1 gramm anyagra.
- Az ozmium tűzállósága miatt feljegyezték az elektromos lámpa történetében. K. Auer von Welsbach német tudós javaslatot tett az izzó szénszálának ozmium izzószálra való cseréjére. Az izzók háromszor kevésbé energiaigényesnek bizonyultak, és a világítás is jelentősen javult. Igaz, hamarosan felváltotta a gyakoribb tantál, amit viszont volfrám váltott fel.
- Hasonló helyzet történt az ammóniagyártás során használt ritka fémmel is. A jelenleg alkalmazott ammóniaszintézis módszer, amelyet 1908-ban a német Fritz Haber vegyész fejlesztett ki, lehetetlen katalizátorok használata nélkül.Kezdetben az akkor használt katalizátorok csak jelentős hőmérsékleti viszonyok mellett mutatták meg tulajdonságaikat, és nem voltak magas hatásfokkal, ezért nagyon sürgős volt a csere keresése. A karlsruhei Higher Technical School laboratóriumának tudósai javaslatot tettek finoman porlasztott ozmium katalitikus elemként való használatára. A vizsgálati eredmények megerősítették, hogy ez az ötlet megéri, a katalitikus hőmérséklet több mint 100 ºC-kal csökkent, és jelentősen megnőtt az ammónia felszabadulása. Igaz, a jövőben megtagadták az ozmiumot, de segített egy ilyen fontos probléma megoldásában.

Az ozmium és más ritka és egyedi fémek játszanak jelentős szerepet tölt be a különböző iparágakban... Még minden mérgező hatása ellenére is megmenti az emberek életét és egészségét.
Az ozmiummal kapcsolatos további információkért lásd a következő videót.








